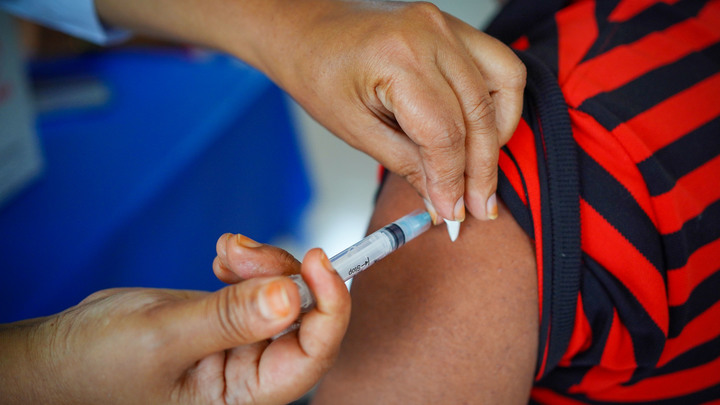
В Pfizer обошли стороной "побочку" при испытании вакцин на детях
Вторая фаза клинических испытаний вакцины, разработанной компаниями Pfizer и BioNTech, на детях завершилась. Создатели препарата отчитались о результатах, но обошли стороной "побочку".
Председатель и главный исполнительный директор Pfizer Альберт Бурла отметил, что за последние 2,5 месяца на 240% выросла заболеваемость COVID-19 среди детей. Именно поэтому в компании убедились в необходимости вакцинации несовершеннолетних. Разработчики препарата надеются, что результаты второй фазы клинических испытаний позволят им в срочном порядке представить в регулирующие органы документы для получения разрешения.
Детей разделили на три возрастные категории: от 0 до 2 лет, от 2 до 5 лет, от 5 до 11 лет. Вторая фаза исследований завершена для третьей из этих групп.
Доза вакцины Pfizer для взрослых составляет 30 мкг. Школьникам вводили по 10 мкг дважды. Интервал составлял три недели. Исследователи считают, что эта дозировка оптимальна с точки зрения безопасности и позволяет получить результат.
В заявлении на сайте Pfizer сказано, что после второй дозы у испытуемых появился "сильный" иммунный ответ. "Побочку" обошли стороной. Говорится лишь, что она "была сопоставима" с той, которая проявлялась в группе людей от 16 до 25 лет.
Детей от 12 лет в США вакцинируют с начала мая. По мнению специалистов американского Управления по санитарному надзору за качеством пищевых продуктов и медикаментов, риски применения препаратов для профилактики COVID-19 ниже, чем преимущества от прививки.